港大醫學院破解胃癌「代謝密碼」 胃癌腫瘤生長減緩最高65%殺癌細胞效率增6倍
關鍵突破:鎖定脂質代謝弱點 腫瘤生長減緩65%
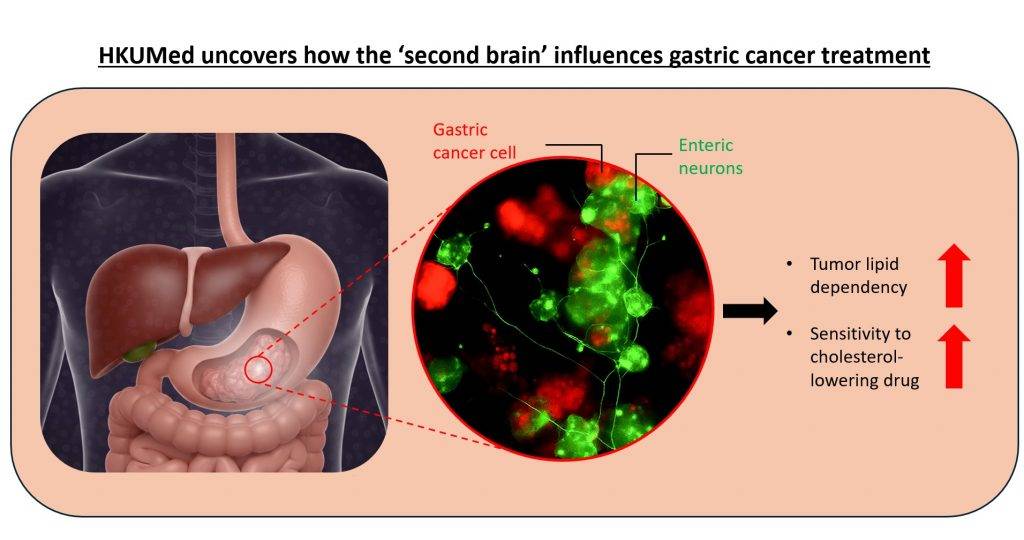
胃癌是全球最致命的癌症之一,由於多數患者在晚期才確診,故存活率一直偏低。除了癌細胞本身,腫瘤還與周邊組織互動,其中負責控制消化功能的腸神經元被發現可促進癌細胞生長。
港大醫學院團隊利用基因編輯技術,掃描細胞中約二萬個基因,最終鎖定兩個脂質代謝相關的關鍵因子,分別為控制脂肪酸的ACACA,及控制膽固醇代謝機制的LSS,這兩個因子就像癌細胞的「能源工廠」,幫助它們製造脂質,維持生長。小鼠實驗結果顯示,透過抑制劑阻斷這些因子,可減緩腫瘤生長速度平均達65%。更關鍵的是,研究團隊開發了模擬腸神經元與腫瘤互動的研究模型,將腸神經元與胃癌類器官共同培養,以模擬患者癌細胞受到神經元滲透的情況。結果發現,癌細胞內的脂肪酸代謝水平明顯升高,換言之癌細胞變得更加依賴脂質。如再配合使用膽固醇抑制劑,殺死癌細胞的效率將可提高6.3倍。
從機制發現到精準治療的轉變契機
領導研究的港大醫學院生物醫學學院副教授黃兆麟教授表示:「我們的研究顯示,腸神經元可以增加胃癌細胞對脂質的需求,而且胃癌細胞更容易受到膽固醇抑制劑的影響。這項發現不僅有助開發胃癌新藥,亦有助制定預測方法了解患者對療效的反應,同時突顯出針對神經元與癌細胞互動作為治療方針的重要性。」

共同領導此研究的港大醫學院臨床醫學學院病理學系系主任梁雪兒教授表示:「研究團隊利用從胃癌患者組織培養的類器官進行基因篩選,揭示了人體第二大腦——腸神經元如何影響胃癌細胞的代謝弱點,這有助理解癌細胞的生長機制,更為開發針對胃癌的精準療法提供了新方向。」
黃兆麟教授補充:「透過識別脂肪酸代謝因子作為潛在生物標記,醫生未來可以更準確有效地為患者配對最適合的治療方案,提升療效和成功率。此方法不僅適用於胃癌,未來還有潛力擴展至其他涉及神經元滲透的癌症,例如胰臟癌或肝癌,為腫瘤微環境研究提供新視角。」
這項發現不僅確立「脂質代謝」作為胃癌藥物開發的新靶點,更為建立預測療效的生物標記系統奠定基礎。研究團隊已就研究成果申請專利,並將進一步拓展模型至其他癌症研究,為癌症精準治療帶來創新突破。